为提升希利斯产品有效性及研究希利斯的免疫持久性,2022年5月22日,康华动保启动了《希利斯临床数据研究试验》。旨在以长期监测的数据反馈市场,给予临床更优质的产品,加强宠物狂犬病的防控工作。
本次试验对康华动保(成都)生物科技有限公司的211012、220101两个批次的希利斯(狂犬病灭活疫 苗)进行犬的免疫试验,每只犬免疫1头份(1 mL)疫 苗,皮下注射,共免疫200只犬,免疫前(0 d)、免疫后第7 d、14 d、21 d和28 d后各采血一次,用动物狂犬病病毒 IgG 抗体定量测定试剂盒(酶联免疫法)进行狂犬病病毒中和抗体测定。同时,观察免疫后30 min内及2 d内不良反应发生情况。
试验涉及犬只品种包含比格犬、泰迪、约克夏、法斗、吉娃娃、柯基、西高地、贵宾、中华田园犬、冠毛犬,共10种。设希利斯免疫组和对照组。其中希利斯免疫组200只,每品种各20只,其中包含10只幼龄犬,10只老龄犬。各品种组内,2个批次希利斯分别免疫幼龄犬5只及老龄犬5只。对照组20只,品种及年龄随机。所有犬只健康状况良好,无其它重大疾病,雌雄随机,狂犬病疫 苗接种史不干预。
本文主要展示《希利斯临床数据研究试验》第一阶段(免疫后0 d、7 d、14 d、21 d、28 d)试验数据,后续试验数据仍在持续跟进中。
免疫后不良反应发生率为0%
免疫后30 min内及2 d内,观察以下不良反应发生情况:
(1)出现注射部位红肿、瘙痒、疼痛,甚至产生硬结;
(2)精 神状态不好,不吃不喝;或者与之前相比过度亢奋;
(3)出现呕吐,频繁排粪、排尿,甚至会便血或者出现排粪困难;
(4)出现全身无力、出汗、不断流涎等现象;
(5)出现昏迷、抽搐、急性休克甚至引起死亡。
试验结果显示,两个不同批次的希利斯免疫试验犬,每只犬免疫1头份(1 mL),皮下注射,免疫后各品种无不良反应产生,其中包含临床上易产生过敏的犬种,如泰迪,约克夏,法斗、柯基等,不良反应发生率为0%。
免疫后7 d检测,所有免疫犬均产生有效狂犬病病毒中和抗体
希利斯免疫组,所有免疫犬7 d后检测,均产生了有效的狂犬病病毒中和抗体(大于等于0.5 IU/mL),其中包含天生存在免疫缺陷的比格犬。对于有/无狂犬病疫 苗接种史的试验犬,均能在免疫后产生有效的狂犬病病毒中和抗体。幼龄犬(3月龄以上)及老龄犬血清中产生狂犬病病毒中和抗体的免疫成功率均为100%。
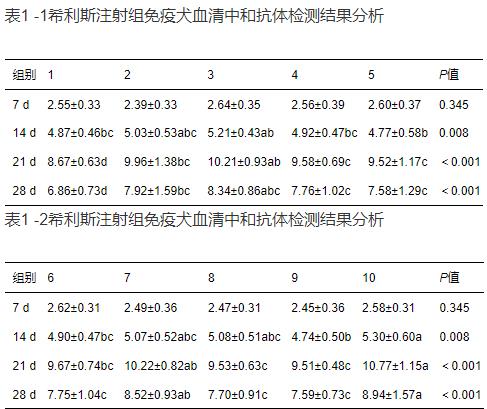
经单因素方差分析,各试验组内血清狂犬病病毒中和抗体水平,免疫后第7天,14天,差异不显著(P值分别为:P=0.871、P =0.925);免疫后第21天,28天,差异显著(P<0.01); 各试验组间血清狂犬病病毒中和抗体水平,免疫后第7天,差异不显著(P =0.345),免疫后第14天,差异显著(P =0.008),免疫后第21天,差异显著(P<0.01),免疫后第28天,差异显著(P<0.01)。具体分析数据见表1-1,1-2。
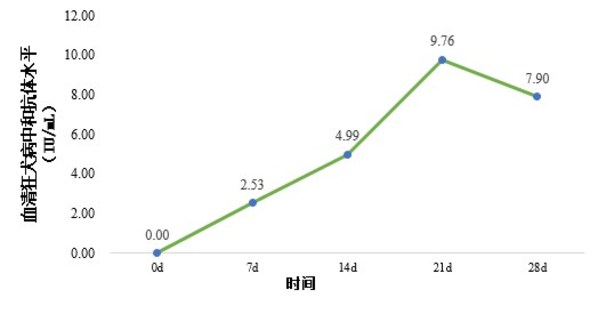
免疫21 d后抗体水平达到峰值
希利斯免疫组,所有免疫犬免疫后21 d左右抗体水平达到峰值,28 d有所下降,但仍具有保护效果。后续数据仍在监测中。
以上试验结果显示,希利斯针对试验犬免疫,试验犬均无不良反应发生,安全性高,且免疫7 d后均产生了有效的狂犬病病毒中和抗体,对试验所涉及的幼龄犬(3月龄以上)及老龄犬均能产生有效的狂犬病病毒中和抗体,免疫成功率为100%。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57