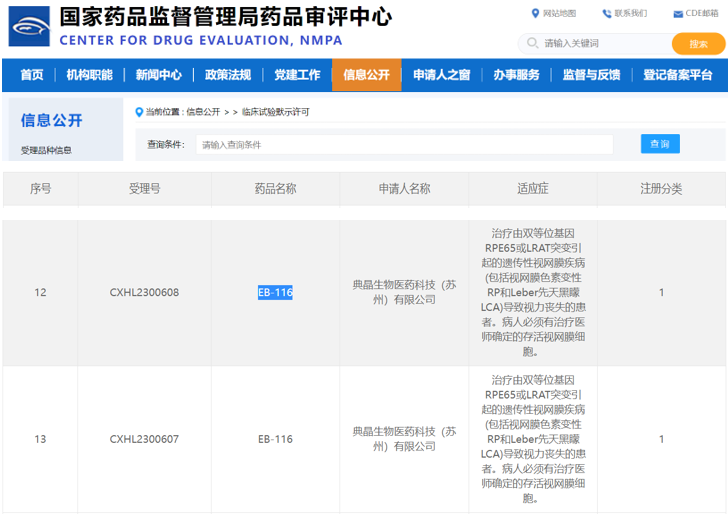
2023年9月5日,根据中国国家药监局药品审评中心(CDE)官网数据显示,典晶生物的1类眼科新药EB-116获临床默示许可,适应症为治疗由双等位基因RPE65或LRAT突变引起的遗传性视网膜疾病(包括视网膜色素变性RP和Leber先天黑矇LCA)导致视力丧失的患者。病人必须有治疗医师确定的存活视网膜细胞。
EB-116(Zuretinol,EB-109)即9-顺视黄醇乙酸酯属于Vitamin A类似物,是一种小分子药物,在体内可转化为9-顺式视黄醛,当被光线刺激后与蛋白结合形成视紫质。2022年典晶生物从Retinagenix Holdings公司收购了Zuretinol资产,包括其全球独占研发和商业化权益。
RPE65或LRAT基因突变导致人体维生素A循环出现严重的缺陷。维生素A在人体转化为11-顺视黄醛(11-cis retinal),用来捕捉光线及引起视觉产生。RPE65或LRAT突变的患者这一关键环节受阻,从而他们的视网膜细胞无法产生视觉,逐渐致盲。
视网膜色素变性(Retinitis pigmentosa,RP)是最常见的遗传性致盲眼病,是指以进行性感光细胞及色素上皮功能丧失为共同表现的遗传性、退行性的疾病,世界范围内发病率1/7000~1/3000,中国发病率约为1/3500。
Leber先天性黑矇(Leber congenital amaurosis,LCA)是发病早而且较为严重的遗传性视网膜病变,全世界患病率为1/81000~1/31000,约占遗传性视网膜变性类疾病的5%,占儿童先天性双眼盲的10%~20%。
在此前披露的8项临床研究中,Zuretinol口服制剂已经在144例受试者中进行了测试,包括健康受试者,隐性RPE65/LCA患者,常染色体显性RPE65患者,以及暗适应受损的早期AMD患者。这些研究均表明Zuretinol具有良好的安全性,耐受性和显著的临床疗效,能够快速改善患者视觉功能。
典晶生物
典晶生物医药科技(苏州)有限公司,(Eluminex Biosciences (Suzhou) Limited) 成立于2020年2月,是一家专注于眼科疾病和重组人胶原蛋白技术的生物医药公司。公司成立3年以来,目前已完成B+轮融资,累计金额超1亿美元。公司进展最快的产品EB-301(生物合成角膜)已进入临床3期。
EB-301是典晶生物从珐博进引进的产品,获得了全球独家开发许可,临床适用于角膜稳定的、非感染性基质病变且需要进行前板层角膜移植术 (ALK) 的病例。中国每年仅进行大约八千例供体角膜移植手术,据估计每年有十五万至二十万名符合角膜移植条件的新患者。









合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57