2024年1月9日, 根据中国国家药监局(NMPA)官网公示,卫材药业递交的1类新药仑卡奈单抗注射液上市申请正式获批。适应症:早期阿尔茨海默病(AD),即确认淀粉样蛋白病理的AD源性轻度认知功能障碍(MCI)和轻度AD痴呆。继2023年7月在美国获得完全批准、9月在日本获得批准后,中国是第三个批准仑卡奈单抗上市的国家。
2023年10月, 仑卡奈单抗已通过海南省药品监督管理局审核,落地海南博鳌乐城国际医疗旅游先行区,商品名为“乐意保”,定价3328.2元/瓶。

作为20年来首 款获得FDA完全批准的AD新疗法,仑卡奈单抗既可选择性地与可溶性Aβ聚合物(原纤维)结合,也可以与Aβ斑块的主要成分不溶性的Aβ聚合物(纤维)结合,从而清除大脑中的Aβ原纤维和Aβ斑块。
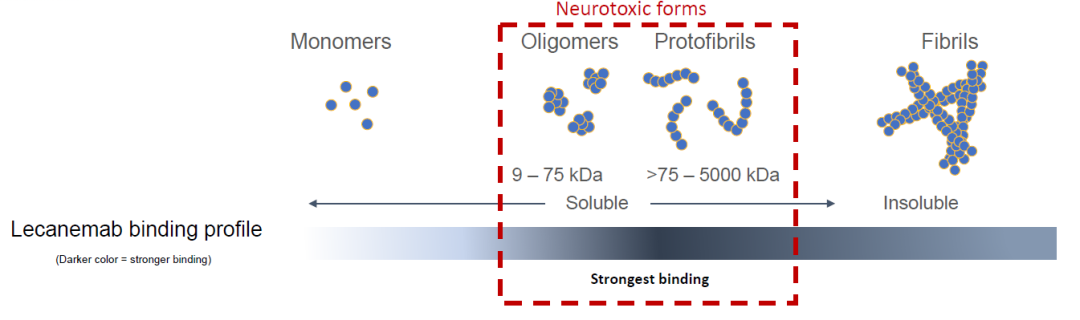
从药渡数据库检索可知仑卡奈单抗(Lecanemab)是由Biogen和卫材合作开发的一款针对阿兹海默症Aβ抗体药物。Lecanemab临床III期研究Clarity AD确认了临床获益:Clarity AD III期临床达到了降低CDR-SB评分主要临床终点和所有关键次要临床终点。在治疗18个月之后,在ITT人群中,Lecanemab相比安慰剂降低了27%的CDR-SB评分(降低了0.45分,p=0.00005)。
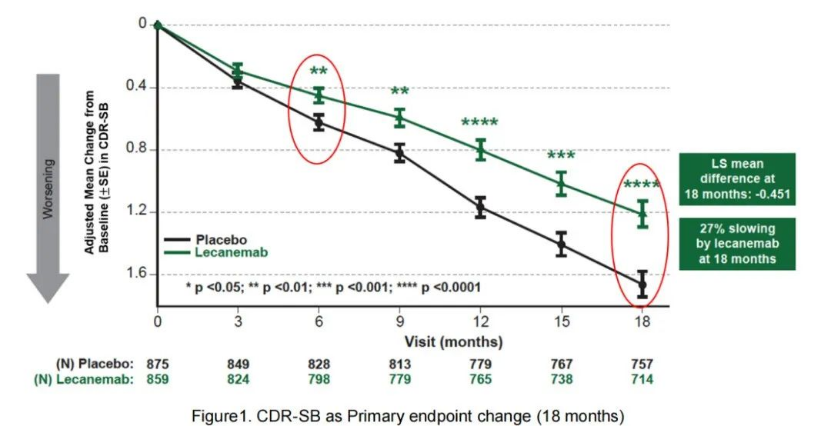
2022年1月6日,Lecanemab获得FDA的加速批准,用于治疗轻度认知障碍或轻度痴呆阶段的AD患者;2023年6月10日,FDA外周和中枢神经系统药物咨询委员会专家以6:0的投票结果支持Lecanemab获得完全批准;2023年7月6日,Lecanemab成为首 个获得FDA完全批准的抗Aβ单抗。
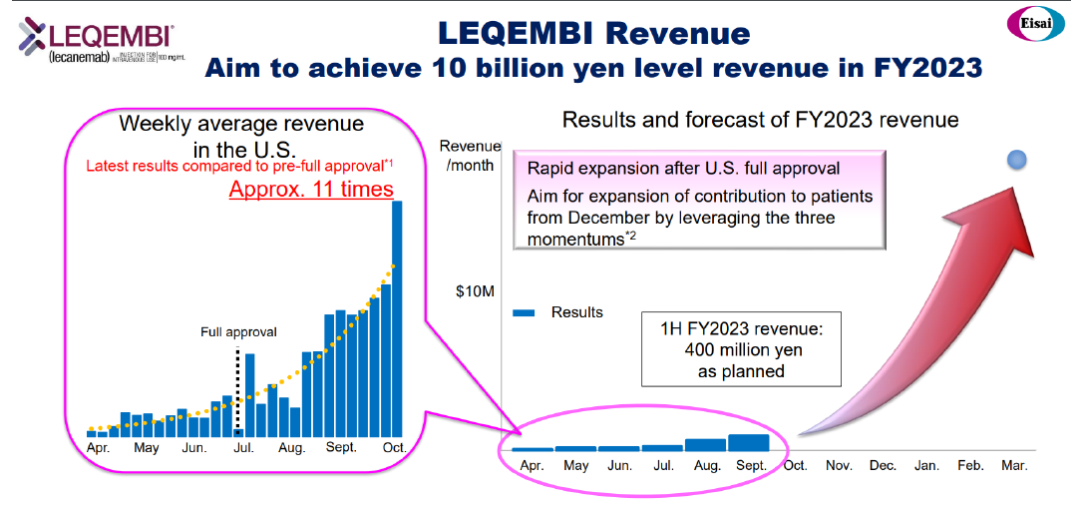
仑卡奈单抗在FDA完全批准之后放量加快。2023年4月-9月,仑卡奈单抗销售额为4亿日元(合265万美元),整个财年目标销售额为100亿日元(约合6600万美元),华尔街部分分析师预测该药销售峰值将达到90亿美金。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57