2月7日,据CDE官网显示,信达生物1类化药新药玛仕度肽注射液的上市申请获得受理。2024年初,信达生物宣布将递交玛仕度肽减重适应症的首 个新药上市申请。
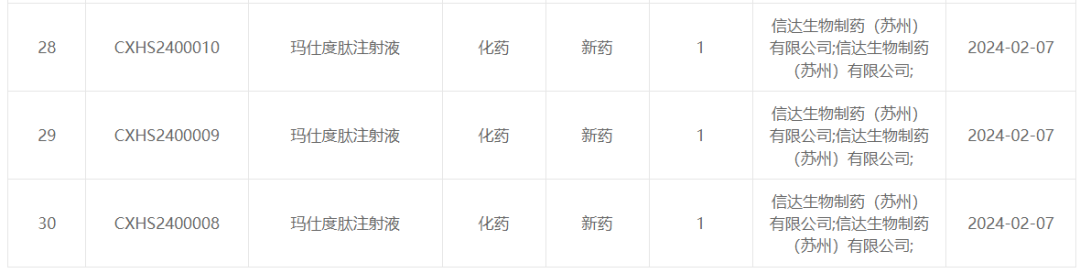
图片来源:CDE官网
01
GLP-1R×GCGR
全球领先
玛仕度肽是信达生物从礼来引进的一款GLP-1R/GCGR双重激动剂,也是全球临床研发进度最快的同类药物。据公开资料显示,玛仕度肽除了GLP-1R激动剂具有的促胰岛素分泌、降血糖和减轻体重等作用外,还有望通过GCGR的激活具有增加能量消耗和改善肝脏脂肪代谢等效应。
2024年1月9日,信达生物公布了玛仕度肽在中国超重或肥胖成人受试者中的首 个III期临床研究(GLORY-1)结果,达成主要终点和所有关键次要终点。据此前新闻稿显示,GLORY-1是玛仕度肽减重适应症的首 个 关键临床研究,能够在进一步证明其疗效和安全性的同时,为中国超重和肥胖人群的减重临床研究领域提供样本量大、质量高且具里程碑意义的临床证据。

图片来源:信达生物
此外,2023年12月26日,信达生物在药物临床试验登记与信息公示平台登记了一项临床试验。该试验是玛仕度肽头对头司美格鲁肽的III期临床试验,用于早期2型糖尿病合并肥胖的中国患者。
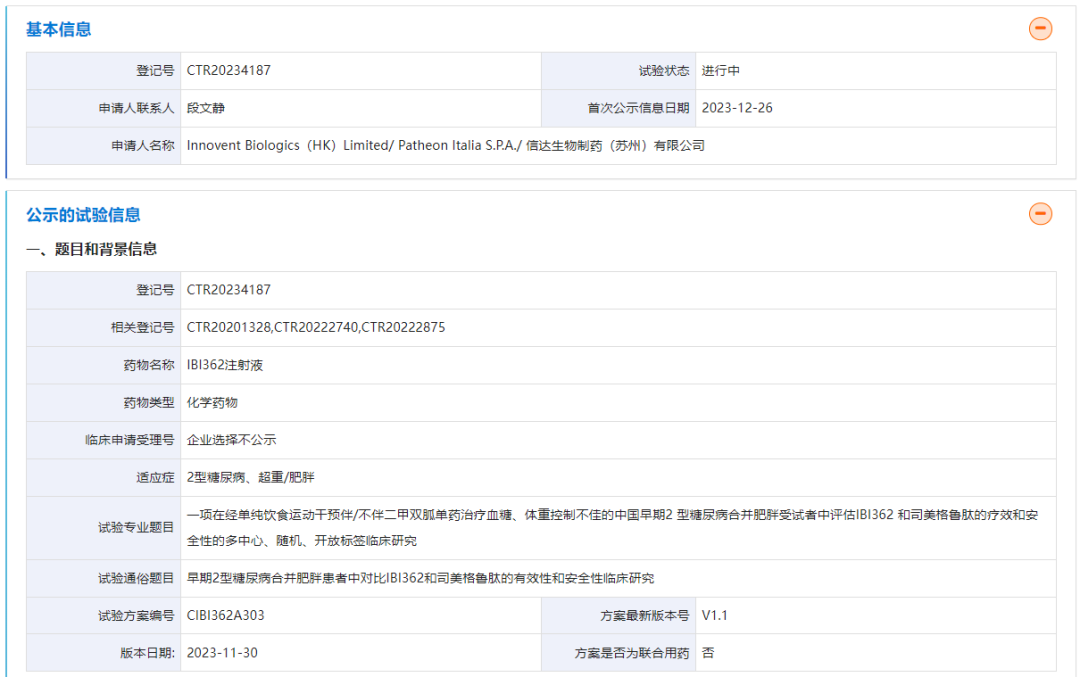
图片来源:药物临床试验登记与信息公示平台
本次玛仕度肽上市申请成功获得CDE受理,有望使其成为全球最领先的GLP-1R/GCGR双重激动剂之一。
02
肿瘤、代谢、自免…
管线布局全面
信达生物专注于高质量生物药开发,已建立起一条包括36个新药品种的产品链,覆盖肿瘤、代谢疾病等多个疾病领域。
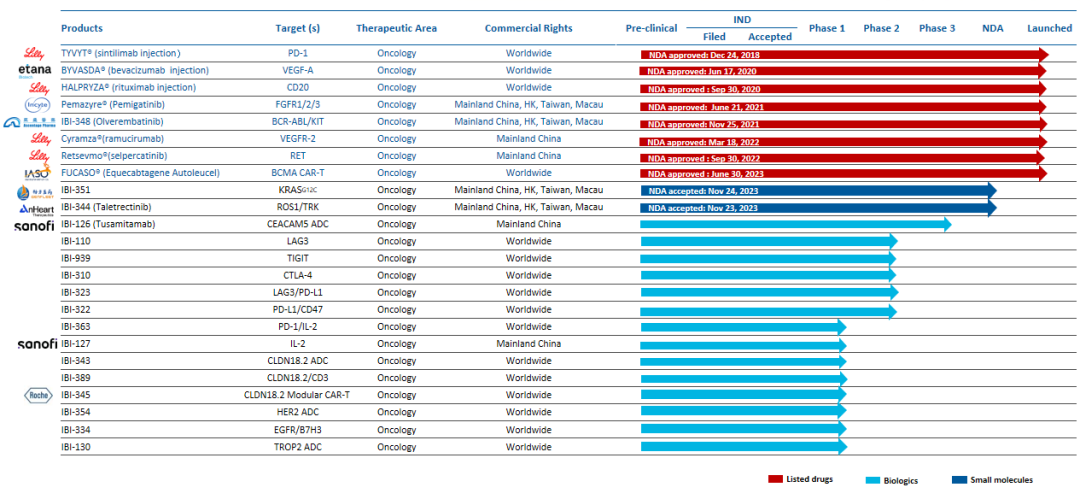
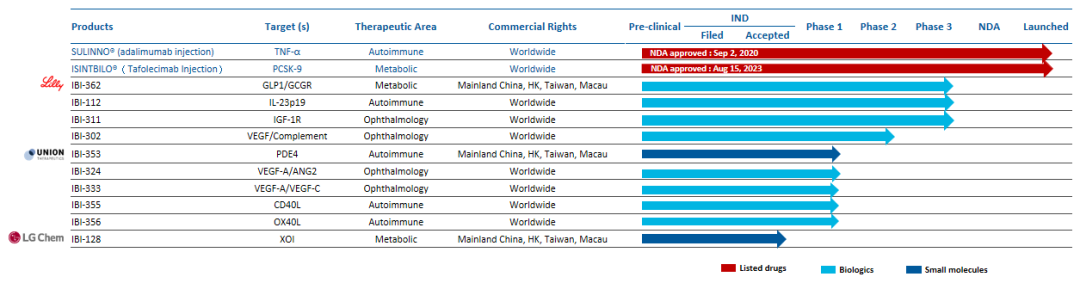
图片来源:信达生物
其中,KRAS G12C抑制剂IBI-351的上市申请已在2023年11月获得CDE受理,该药物是中国首 个 递交NDA的KRAS G12C抑制剂。同月,信达生物新一代 ROS1 TKI泰莱替尼的新药上市申请也获得CDE受理,用于经ROS1-TKI治疗失败的ROS1 阳性局部晚期或转移性非小细胞肺癌成人患者的治疗。
03
结语
玛仕度肽作为全球领先的GLP-1R/GCGR双重激动剂,有望为广大肥胖人群带来更多临床用药选择。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57