2月22日 ,信达生物宣布,创新药物PD-1抑制剂达伯舒®(信迪利单抗注射液)正式获得中国澳门药物监督管理局(ISAF)批准上市。
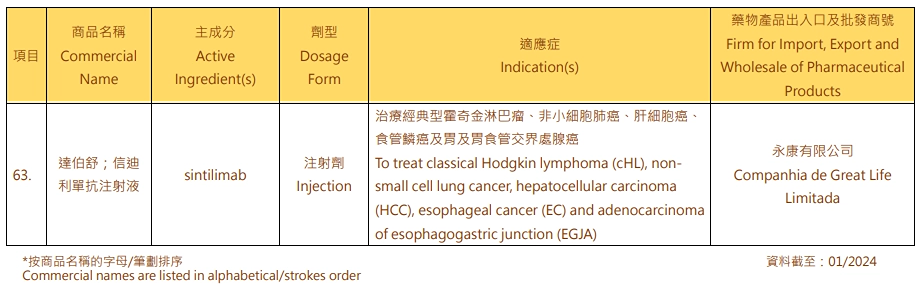
达伯舒®(信迪利单抗注射液)由信达生物和礼来制药共同合作开发,2018年12月24日在中国大陆获批上市,目前已获批七项适应症,涵盖非鳞状非小细胞肺癌、鳞状非小细胞肺癌、EGFR突变非鳞状非小细胞肺癌、肝癌、胃癌、食管癌、霍奇金淋巴瘤。达伯舒®是唯一将五大高发瘤种一线治疗均纳入国家医保目录的PD-1抑制剂,也是中国首 个且目前唯一胃癌一线全人群医保的PD-1抑制剂。
信达生物制药集团高级副总裁周辉博士表示:“此次在澳门的批准是达伯舒®临床开发又一里程碑,拓宽了达伯舒®药物应用地区,扩大了澳门居民临床用药覆盖范围,更多患者因此受益。我们将积极配合各地区监管,推进药物创新,为更多癌症患者带来福音。信达生物始终秉承‘开发出老百姓用得起的高质量生物药’的使命,深耕药物创新,努力为实现‘健康中国2030’添砖加瓦,为推进大湾区的健康事业发展不断做出贡献。”
信迪利单抗,中国商品名为达伯舒®(信迪利单抗注射液),是信达生物制药和礼来制药共同合作研发的具有国际品质的创新PD-1抑制剂药物。信迪利单抗是一种人类免疫球蛋白G4(IgG4)单克隆抗体,能特异性结合T细胞表面的PD-1分子,从而阻断导致肿瘤免疫耐受的 PD-1/程序性死亡受体配体1(Programmed Death-Ligand 1, PD-L1)通路,重新激活淋巴细胞的抗肿瘤活性,从而达到治疗肿瘤的目的i。
信迪利单抗已在中国获批七项适应症并全部纳入国家医保目录,协议期内医保目录描述的限定支付范围包括:
至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗;
表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗;
表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗失败的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者的治疗;
不可手术切除的局部晚期或转移性鳞状非小细胞肺癌(NSCLC)的一线治疗;
既往未接受过系统治疗的不可切除或转移性肝细胞癌的一线治疗;
不可切除的局部晚期、复发或转移性食管鳞癌的一线治疗;
不可切除的局部晚期、复发或转移性胃及胃食管交界处腺癌的一线治疗。
信迪利单抗另有两项临床试验达到研究终点,包括:
单药用于晚期/转移性食管鳞癌二线治疗的II期临床研究;
单药用于含铂化疗失败的晚期鳞状非小细胞肺癌二线治疗的III期临床研究。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57