




5月13日,国家药监局发布《2025年度药品审评报告》显示,2025年,全年批准上市创新药76个品种,其中新机制新靶点药物11个。新批准罕见病用药48个品种,批准儿童用药138个品种。创新药研发遵循著名的"双十定律"——研发一款新药通常需要耗时10年、投入10亿美元,且成功率仅为10%,这充分体现了创新药开发的高风险、高投入特性。尽管面临诸多挑战,中国创新药市场依然展现出强劲的增长势头。据中商产业研究院预判,2025年中国创新药市场规模将增长至约1.22万亿元人民币,同比增长约8%。纵观近十年,在全球医药市场快速发展的今天,中国的医药市场始终健康稳定推进,创新药的审批上市速度更是明显加快。
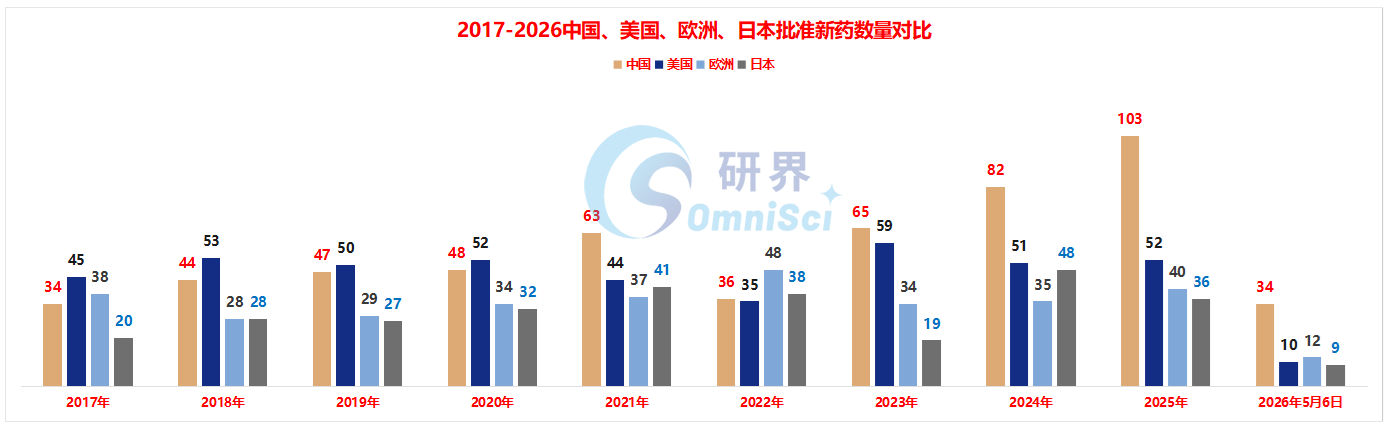
数据来源:药渡数据
从上图可以看出,2017-2026近十年以来,中国批准的新药数据平均每年是55.6个,美国批准的新药数据平均每年是45.1个,欧洲批准的新药数据平均每年是33.5个,日本批准的新药数据平均每年是29.8个,整体来看,近十年以来,中国批准的新药数据年均值最高,美国第二,欧洲第三,日本第四。
注:本文两张图片中所列新药是指NMPA首次批准在中国上市的药品,包括新分子实体(以及包含有新分子实体的复方)。新分子实体主要是化药注册分类下的1类和5.1类;生物药主要为NMPA首次批准的国产及进口生物药;不包含化学仿制药、疫苗、血液 制品、生物类似药、新适应症、新剂型、新给药途径和改变适用人群等情形。
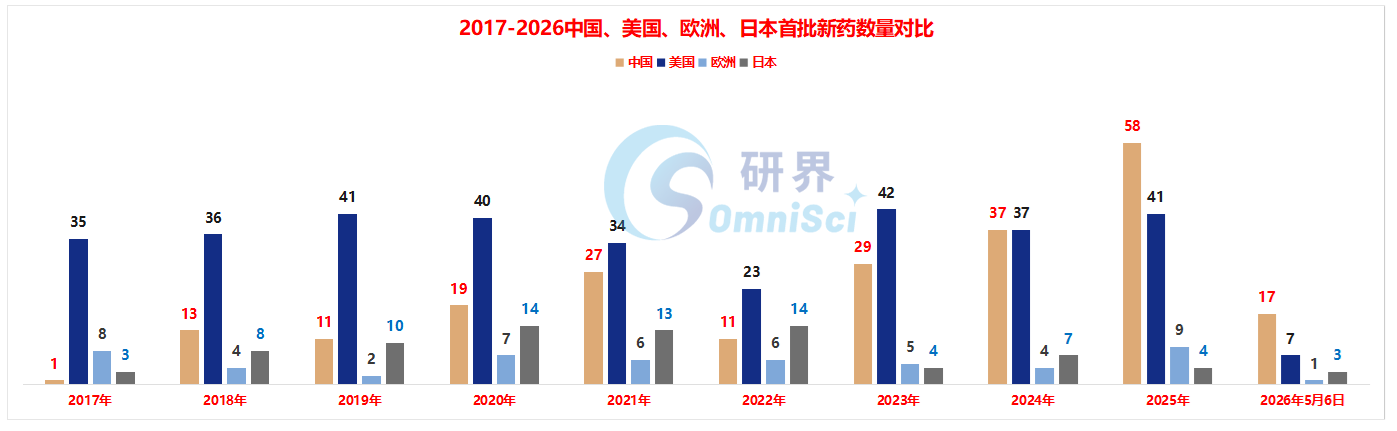
数据来源:药渡数据
从上图可以看出,2017-2026近十年以来,中国首批的新药数据平均每年是22.3个,美国首批的新药数据平均每年是33.6个,欧洲首批的新药数据平均每年是5.2个,日本首批的新药数据平均每年是8个,整体来看,近十年以来,美国首批的新药数据年均值最高,中国第二,日本第三,欧洲第四。
据有关数据显示,2018-2020年,我国新药临床试验数量为2758条,其中化药占比60%。2021-2023,我国新药临床试验数量为5216条,抗体偶联药物(ADC)的临床试验数量占比从1.8%提至4.9%,以基因疗法、溶瘤病毒、细胞治疗为代表的创新疗法占比也在提高。
回顾过往,中国的创新药市场,以2015年国务院发布的《关于改革药品医疗器械审评审批制度的意见》为拐点,整体迎来快速的爆发期,期间一系列核心政策(临床试验申请默许制、加入ICH、优先审评审批、MAH制度试点)的出台,以及相关重磅产品的发力上市(PD-1/PD-L1抑制剂、CAR-T细胞疗法、ADC(抗体偶联药物)),极大地推动了中国创新药市场的发展。以最近国办下发的《关于健全药品价格形成机制的若干意见》有关政策为例,《意见》在创新药获批上市后的各个环节,进一步精准提出了支持措施:药品首 发阶段,启动优化首 发价格机制;药品进入医保阶段,将继续优化医保目录调整规则,兼顾患者获益和鼓励创新,谈判形成的医保支付标准要合理体现药品的临床价值,在药品参与集采阶段,《意见》也强调集采不涉及创新药,也就是我们常说的“创新不集采,集采非创新”。
在政策、数据、产业三重势能的加持下,中国临床数据的价值被前所未有地激活,成为驱动创新的核心引擎。然而,仅有引擎是不够的,一辆能驰骋全球的“中国创新车”,还需要一套精密的“全球运营系统”,这套系统的核心,是构建从研发到商业化的全链条“价值链出海”能力。在研发端,我们看到的是一场“头脑风暴”的全球化,中国药企正从封闭走向开放,通过海外研发布局与国际合作,直指全球科学最前沿的目标——开发出定义未来的“First-in-class”药物。
在临床端,这更是一场“硬仗”的全球化。面对FDA、EMA等严格的监管,中国企业不再是“考生”,而是“命题者”和“考官”的角色。百济神州的泽布替尼,凭借其自主设计的全球多中心头对头试验,用无可辩驳的数据证明了其优越性,实现了在欧美市场的“现象级”获批。这标志着,中国创新药企已具备定义和引领国际标准的能力。这不再是简单的“出海”,而是中国创新价值在全球范围内的体系化输出。据有关数据显示,2025年,中国创新药对外授权交易总金额达到1356.55亿美元,首付款70亿美元,交易总数量157起,中国创新药交易额已占全球总额的49%,全年对外许可总金额为2024年的2.5倍,是美国同期对外许可的3.2倍。
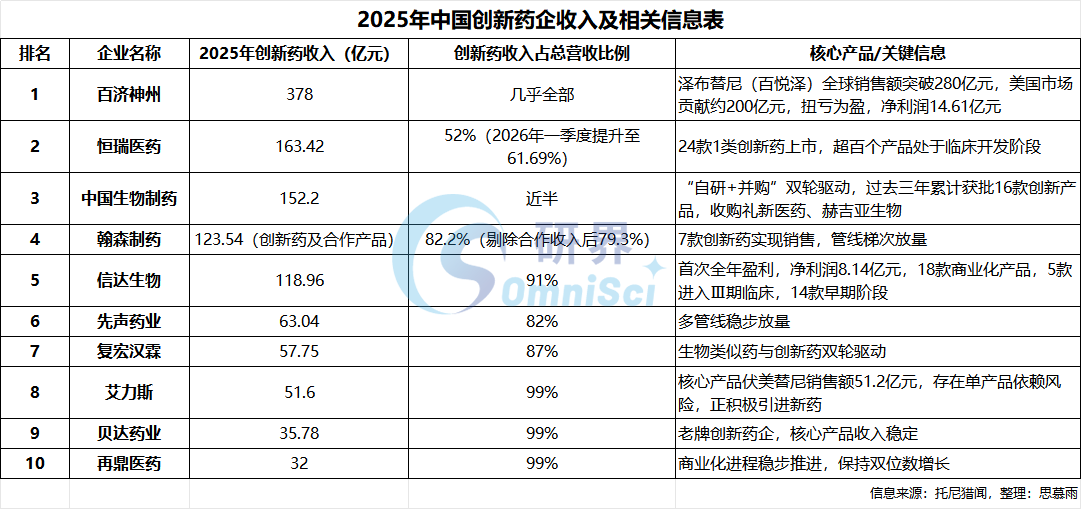
在生产与商业化端, “一带一路”倡议为中国药企的国际化提供了广阔的舞台。通过在东南亚、中东、非洲等地建立符合国际标准的生产基地,不仅可以规避贸易壁垒,实现本地化生产,更能深度融入当地市场,构建起覆盖全球的供应链体系。同时,通过 License-out(对外授权)模式的成熟运用,中国药企可以在早期阶段就将海外权益授权给实力雄厚的跨国药企,借助其全球销售网络实现市场覆盖,这不仅能获得可观的首付款和里程碑付款,为后续研发输血,更能学习先进的商业化经验,为自有产品的出海铺平道路。
笔者认为,今后药品的价值将回归其本质——临床价值与创新程度。高水平的创新药因其高投入、高风险的特性,将获得价格保护的倾斜;改良新药则需证明其独特的临床获益才能获得市场溢价;而通用名药则将在充分竞争的集采市场中实现价值发现。这种精细化分类,标志着国家对药品价值的评估进入了更为科学和精准的阶段,对创新药来说更是一种利好。
 ×
×