https://www.cphi.cn 2023-11-23 16:02 来源:药智头条 作者:米朵
一款创新药从研发立项到成功进入市场,需要经历10到15年的时间,耗资可达数十亿美元,所花费的时间之长,成本之高,都是药企需要面临的挑战,这也是First in Class药物难以成功的原因。
对于多数药企,在创新药物的未知探索之旅中,虽说失败也是常态,但是面对接二连三的失败和接踵而来的舆论压力,是坚持到底还是另辟蹊径?今年以来,FibroGen(珐博进)就这样的灵魂拷问中奋力前行。
Pamrevlumab三度折戟
2023年8月30日,Fibrogen宣布CTGF抗体Pamrevlumab治疗杜氏肌营养不良症(DMD)的非卧床患者的Ⅲ临床LELANTOS-没有达到NSAA主要终点和关键次要终点,这是Pamrevlumab今年以来遭遇的的第三次临床失败。
此次没有达到NSAA总评分从基线到第52周变化的主要终点(安慰剂校正平均差-0.528分;95% CI -2.308 - 1.251;p = 0.5553)。在第52周从基线的变化中测量的次要终点,4级楼梯爬速度,10米步行/跑步测试,站立时间,失去活动时间,以及在10米步行/跑步测试中超过10秒的患者比例也未达到。
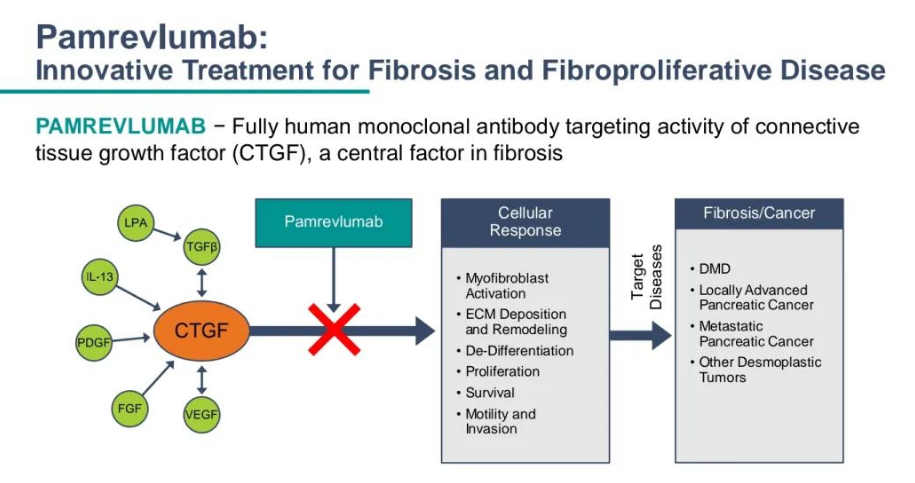
Pamrevlumab是FibroGen开发的一款全球首 创的靶向CTGF的first-in-class抑制剂,CTGF是纤维化和增殖性疾病的常见因子,疾病表现为持续和过度瘢痕,可导致器官功能障碍和衰竭。CTGF抑制剂通过抑制CTGF活性以治疗特发性肺纤维化(IPF)、局部晚期不可切除胰腺癌(LAPC)和杜氏肌营养不良症(DMD)。
FibroGen对Pamrevlumab寄予厚望,进行了多项临床开发,包括特发性纤维化(IPF)、胰腺癌(LAPC)、杜氏肌营养不良(DMD)这3个适应症均到达III期临床阶段。此前,FDA已授予pamrevlumab孤儿药认定和快速通道认定,用于治疗LAPC和DMD患者,FDA还授予pamrevlumab罕见儿科疾病认定,用于治疗DMD患者。
遗憾的是,Pamrevlumab各个适应症的研发进入临床III期后,开始出现一系列的问题,除此次治疗DMD的LELANTOS-2的失败,此前,Pamrevlumab已经叫停了两项III临床研究。
今年6月7日,FibroGen宣布Pamrevlumab治疗12岁以上非卧床杜氏肌营养不良(DMD) Ⅲ期临床试验LELANTOS-1失败。结果显示,与基线相比,Pamrevlumab+皮质类固醇激素治疗组并未在第52周达到上肢功能2.0(PUL 2.0)评分改善的主要终点。
紧接着,6月26日,Pamrevlumab治疗特发性肺纤维化的Ⅲ期临床ZEPHYRUS-1宣告失败,主要终点和次要终点均未达到,这个结果迫使FibroGen终止了另一项名为ZEPHYRUS-2的Ⅲ期临床研究。
IPF和DMD两大适应症接连失败,目前Pamrevlumab只剩LAPC一个适应症在推进,根据FibroGen透露,针对LAPC的LAPIS3期研究数据将于2024年上半年出报告,同时Pamrevlumab治疗转移性胰腺癌的实验目前进展到Ⅱ/Ⅲ期阶段。此外III期 LELANTOS-2 试验中来自DMD的门诊患者的数据将于三季度公布,我们期待针对胰腺癌的LAPIS3期能带来意外的转机。
裁员降本
作为FibroGen管线的主要候选物,Pamrevlumab接二连三的Ⅲ期临床失败,让FibroGen元气大伤,再加上FibroGen唯一一款看家产品roxadusta(罗沙司他)因为无法在骨髓增生异常综合征患者中实现红细胞输注独立性方面与安慰剂显著区分在今年5月的临床Ⅲ期试验失败,FibroGen股价和市值遭遇重创,FibroGen走到了低谷。
不过,FibroGen迅速采取措施进行自救:裁员降本。
7月19日,FibroGen对外宣布了一项人员重组计划:为了降低运营成本,珐博进将削减其美国团队约32%,即104名员工。

据公告,裁员将在2024年第一季度末基本完成,将用1300万至1500万美元用于员工遣散费等,剩余大部分费用将在2023财年的第三季度产生,费用支付与裁员基本可以同步完成。
FibroGen预计,通过裁员,将节省3000万至3500万美元的年度费用,目前,珐博进的现金及现金等价物等足够支持公司开支到2026年。
在裁员公告发布的一周后,FibroGen的CEO Enrique Conterno(康特诺)宣布“因个人原因”辞职,但新的临时首席执行官塔那·韦蒂格接任,康特诺在过渡期将辅助塔那·韦蒂格监督抗体Pamrevlumab III期研究的进行。
守住中国市场
FibroGen创始于1993年,如今已走过三十年,主要关注结缔组织生长因子(CTGF)和缺氧诱导因子(HIF)的生物学研究和创新药物开发。2014年11月FibroGen迎来高光时刻,在纳斯达克上市,目前FibroGen只有一款新药上市罗沙司他(roxadustat)。
2018年12月,罗沙司他全球范围内率先在中国获批上市,商品名为爱瑞卓;,是第一款外资药企研发并在中国完成全球首 发的HIF-PHI创新药物,相比传统肾性贫血治疗药物,HIF-PHI更有效,且仅需口服给药,患者依从性高,药物一经上市,备受患者青睐。
2019年8月,用于非透析依赖性CKD患者的贫血治疗的适应症获得NMPA批准;2019年11月,罗沙司他通过国家医保谈判纳入医保;2021年又通过医保降价谈判降,价格降了近一半;2022年罗沙司他作为国谈药品列入“双通道”药品管理。
根据珐博进财报,经历医保降价谈判,罗沙司他2021年全年为营收13.17亿元,同比增长约12%,销量增长超80%;2022年销量稳步增长,净销售额为约14.6亿元,成为了销量逼近15亿元的大单品。2023上半年,罗沙司他销售10.32亿元,半年就已突破10亿,其中2023Q2销售5.32亿元,同比增长44%,市场前景良好。
罗沙司他在国内无论是申请审批,医保谈价,医院销售都是一路顺风顺水,在中国一定是开启了罗沙司他的肾性贫血的“新时代”,在当下的国内HIF-PHI药物领域独占鳌头。
除了中国之外,FibroGen将罗沙司他的版图拓展到了日本、智利、欧盟等国家地区,其中日本是在2019年获批上市,欧盟地区是2021年获批。
不过罗沙司他在日本和欧洲的商业化并不顺利,FibroGen的合作伙伴Astellas最近根据黯淡的销售预测,日本只为罗沙司他计入了价值470亿日元(合3.48亿美元)的减值支出。
另外,再加上罗沙司他由于安全性问题,一直被FDA拒之门外,因此,罗沙司他主要的销售收入来源于中国国内。
但是,信立泰的恩那司他于今年6月获国家药监局批准上市,随着信立泰的入局,罗沙司他在国内的垄断局面被打破,未来或将面临来自恩那司他的的竞争,同时,罗沙司他化合物专利、组合物专利和医药用途专利到期时间均为2024年6月4日,目前国内多家企业报产仿制药,未来一两年时间,罗沙司他还将面临来自仿制药的冲击。
不过,FibroGen也对此积极应对,今年5月,FibroGen宣布罗沙司他在中国进行的又一项III期临床研究取得了积极的关键数据,该研究评估了对于正在接受化疗的非髓系恶性肿瘤受试者,使用罗沙司他治疗贫血的有效性和安全性。
相信FibroGen会不遗余力持续深耕并守住中国市场。
切入ADC领域
Pamrevlumab的杜氏肌营养不良(DMD)和特发性肺纤维化(IPF)两项适应症中遭遇后期失败,市场开始质疑CTGF抗体的治疗前景。实际上FibroGen并不是第一家在CTGF抗体遭遇后期失败的企业,以IPF适应症为例。
IPF是一种罕见的慢性进行性肺部疾病,患者长期预后较差,5年生存率仅为20%。自2014年两种抗纤维化药物吡非尼酮(Pirfenidone)和尼达尼布(Nintedanib)上市以来,还没有任何新药被批准用于该适应证。
2019年,罗氏以3.9亿美元预付款收购了Promedior公司获得后者的纤维化治疗产品组合。其中,针对IPF的资产zinpentraxin alfa是整笔交易的核心。当时该药已经获得了FDA的突破性疗法认定。但在2022年财报中,罗氏透露,已经停止了zinpentraxin alfa的关键III期试验。
因此FibroGen也需要在Pamrevlumab外探索更多可能。
除Pamrevlumab的相关临床试验,FibroGen表示今年底和2024年第一季度提交研究性新药申请IND - 启动两种抗体的抗肿瘤的临床项目。它还预计将在明年下半年开始FG-3246在转移性,去势抵抗性前列腺癌中的中期临床试验。
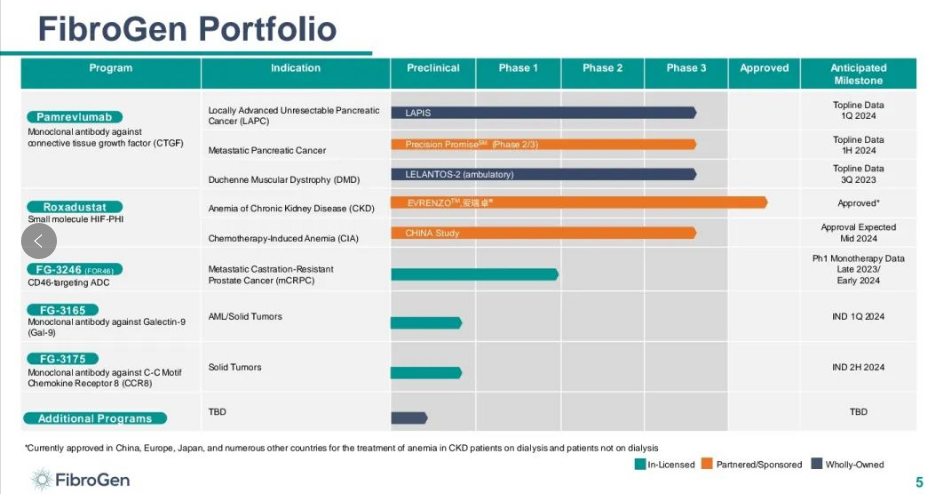
此外,今年5月8日,FibroGen宣布与Fortis合作,以高达2.8亿美元引进一款在研CD46 ADC,FOR46,用于转移性去势抵抗性前列腺癌(mCRPC)和其他CD46表达的癌症。
FibroGen借此切入大火的ADC赛道,只是目前CD46刚进入I期临床,ADC能否为FibroGen再下一城,我们拭目以待。
对于当下的FibroGen,路虽难走,但依旧值得期待。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030