2023年11月24日,云顶新耀宣布中国国家药品监督管理局(NMPA)已批准耐赋康®(Nefecon®,布地奈德迟释胶囊)的新药上市许可申请(NDA),用于治疗具有进展风险的原发性IgA肾病成人患者。
2019年6月,云顶新耀与 Calliditas 签订独家授权许可协议,获得耐赋康®在大中华地区和新加坡开发以及商业化权利。该协议于2022年3月扩展,将韩国纳入授权许可范围。根据药渡数据检索目前,耐赋康®于2021年12月首次在美国获批;2022年7月在欧盟获批;今年10月27日在中国澳门获批。
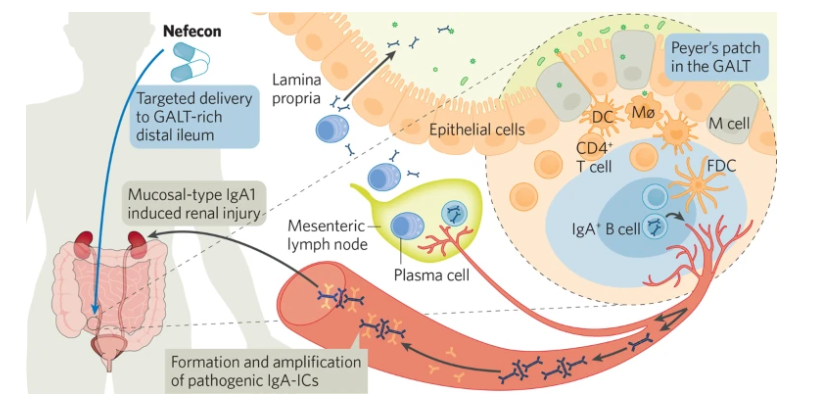
虽然IgA肾病表现为肾脏问题,但该疾病被认为起源于小肠。回肠中的特殊淋巴组织称为派尔集合淋巴结,是B淋巴细胞分化的场所,导致致病性分泌型IgA1抗体的产生。在IgAN患者中,这些IgA抗体进入体循环,它们的存在会引发自身免疫反应,并导致形成沉积在肾脏中的免疫复合物。
耐赋康®是靶向肠道的黏膜免疫调节剂,其通过特殊的制作工艺,将布地奈德(糖皮质激素的一种)靶向释放于回肠末端的黏膜B细胞(包括派尔集合淋巴结),胶囊溶解后,三层包衣微丸持续稳定释放布地奈德,高浓度覆盖整个靶区域,从而减少诱发IgA肾病的半乳糖缺陷的IgA1抗体(Gd-IgA1)产生,进而干预发病机制上游阶段。
2023年11月美国肾脏病学会肾脏周(ASN kidney week)公布了耐赋康®临床3期的研究结果,数据显示:
中国亚组数据显示了耐赋康®在肾功能保护、蛋白尿下降和镜下血尿改善等方面疗效较全球人群更优,在2年的治疗和观察期间:
1)中国亚组治疗组时间加权的eGFR平均下降3.7ml/min/1.73㎡,而安慰剂组时间加权的eGFR平均下降13.3ml/min/1.73㎡,耐赋康®治疗可带来9.6ml/min/1.73㎡的eGFR获益,而全球人群的治疗获益(5.1ml/min/1.73㎡)。
2)中国人群中eGFR在24个月时较基线的平均绝 对变化表明,耐赋康®治疗的患者肾功能恶化程度较安慰剂减少了约66%,这一数值在全球人群约为50%。
3)中国人群经过9个月治疗在9个月和24个月时分别使尿蛋白肌酐比值(UPCR)降低31%和43%。而全球人群在9个月与24个月时约下降30%。
4)中国人群中,耐赋康®组2年内无镜下血尿的患者比例从基线的26.9%提升至57.7%,而安慰剂组无变化。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57