https://www.cphi.cn 2018-01-03 09:41 来源:转载
品种
利拉鲁肽一路上扬
利拉鲁肽是诺和诺德研发的GLP-1受体激动剂,2010年1月25日获得FDA批准,商品名为Victoza。
利拉鲁肽为人GLP-1结构链的34位Lys被Arg取代,在26位的Lys上接入经16烷酸修饰的谷氨酰胺。GLP-1经脂肪连修饰后,增加了与白蛋白之间的亲和力,从而降低了被DPP-Ⅳ酶的水解速率和肾清除率,延长生物半衰期。利拉鲁肽的消除半衰期为13小时,每日只需注射一次。
这一优势带动利拉鲁肽市场一路上扬,2016年全球利拉鲁肽市场达到29.80亿美元,同比上一年增长11.20%。
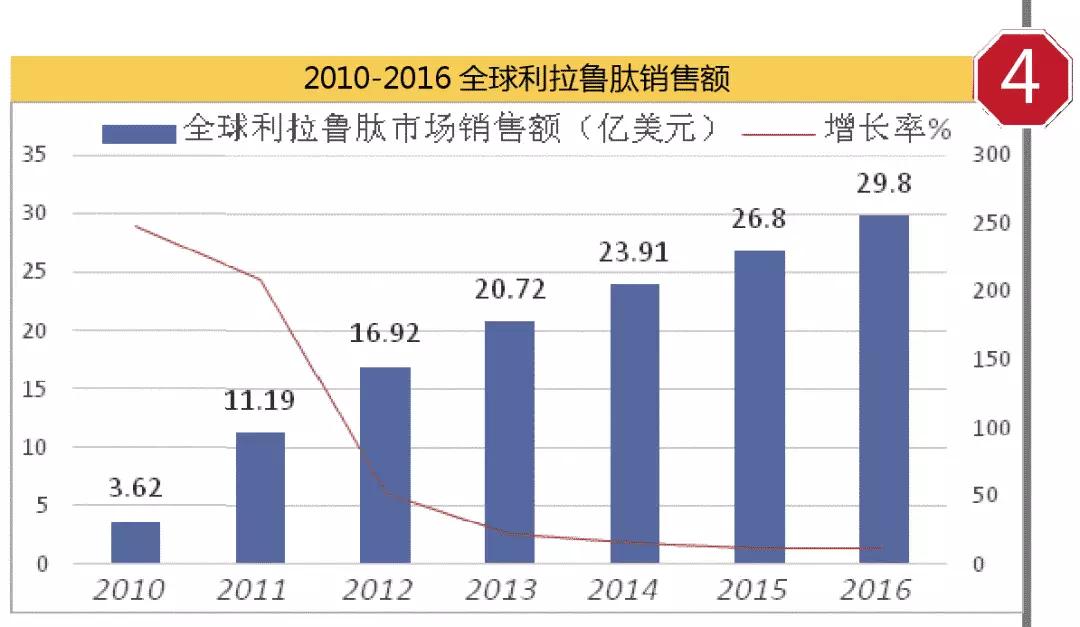
2011年,利拉鲁肽在中国上市,商品名为诺和力。据米内网数据,2016年国内重点城市公立医院诺和力市场为2691万元,同比上一年增长43.83%。按照2017年前3季度数据测算,2017全年或将达到3276万元,同比上一年增长21.74%。
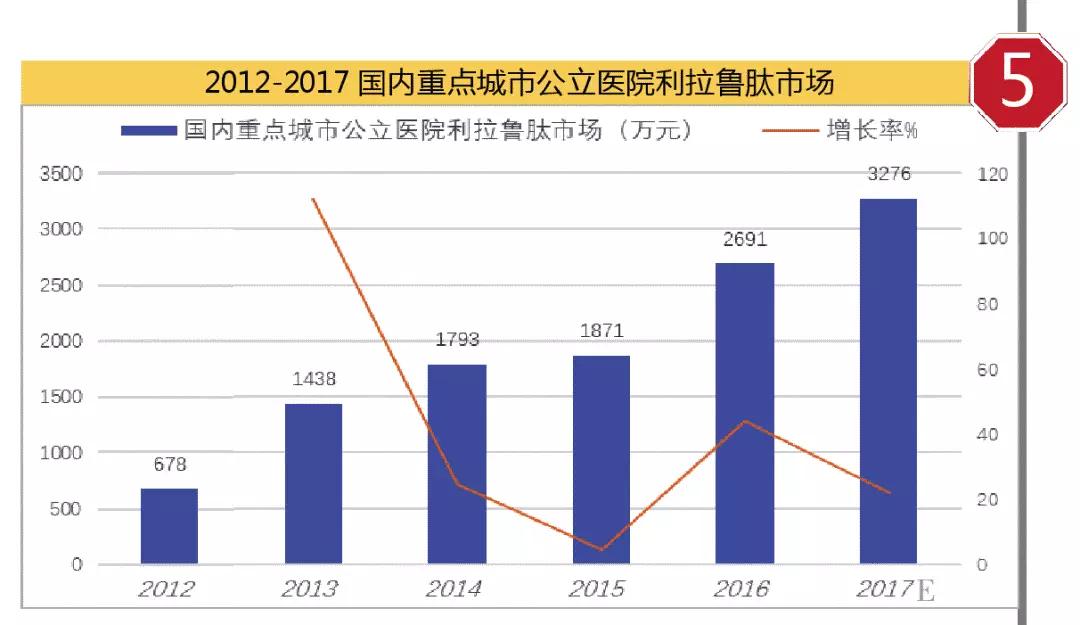
艾塞那肽恐下滑
艾塞那肽是从蜥蜴唾液中分离出的GLP-1类似物,由39个氨基酸组成,与人GLP-1有53%的同源性。
2005年4月,艾塞那肽获得FDA批准上市,商品名为Byetta。艾塞那肽能降低2型糖尿病患者糖化血红蛋水平和餐后血糖,并能减轻体重,平均半衰期只有2.4小时,每天需注射2次。为提高患者的顺应性,2012年艾塞那肽缓释微球上市,一周仅注射一次,商品名为Bydureon。2016年艾塞那肽全球市场为11.47亿美元,同比上一年下降1.12%。
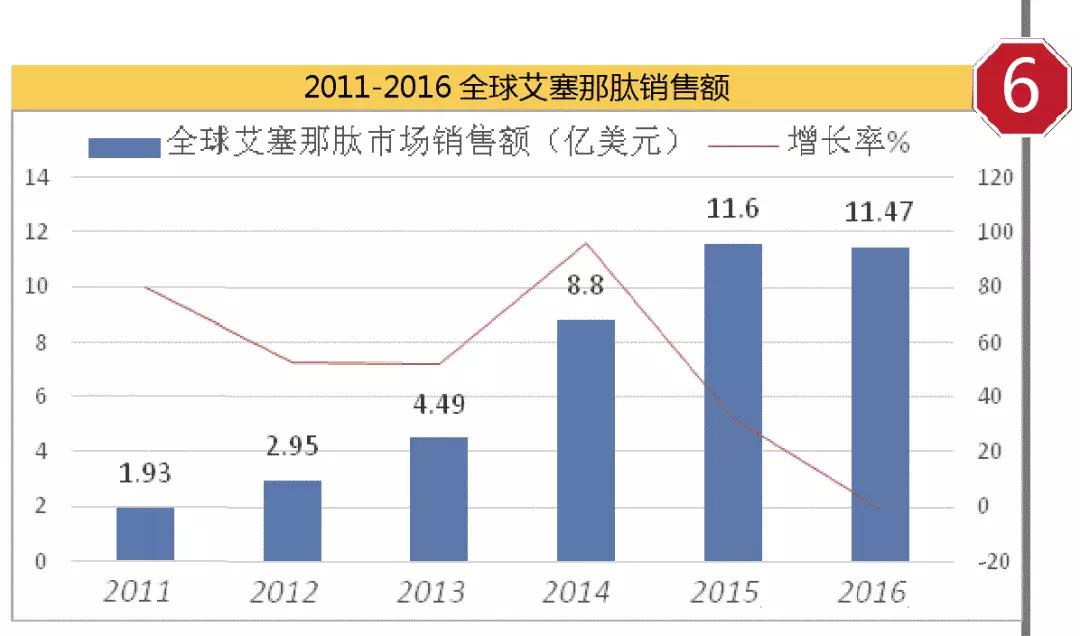
2009年8月阿斯利康的艾塞那肽在中国获批上市,由Baxter生产,商品名为百泌达。据米内网数据,2016年国内重点城市公立医院百泌达市场为2718万元,按照2017年前3季度数据测算,2017全年或下降至2586万元,原因可能是每日注射两次削弱患者用药依从性,呈现出下滑趋势。
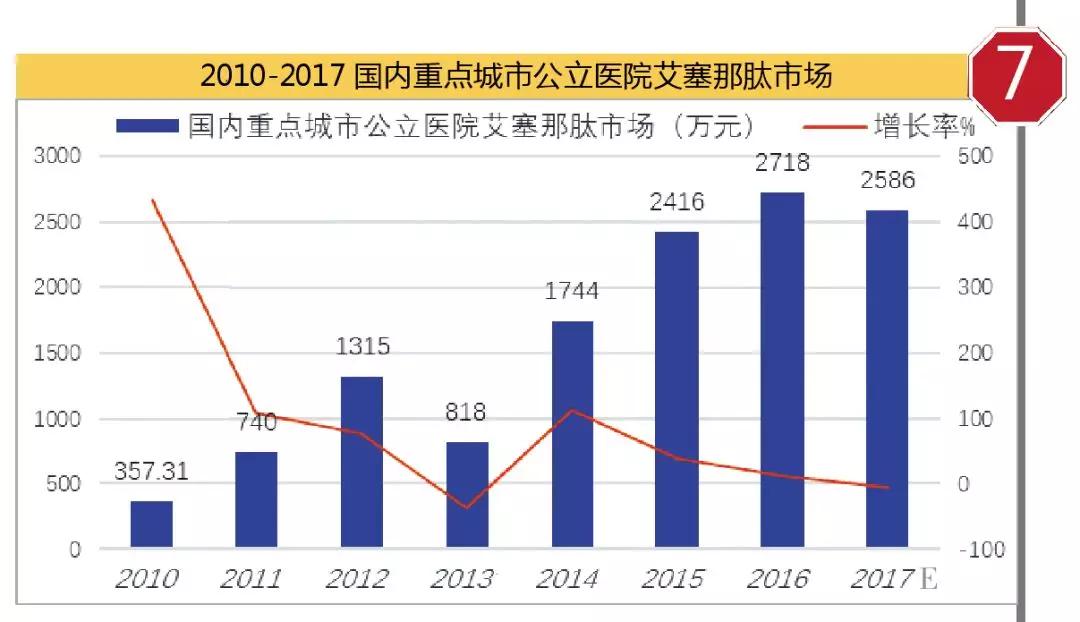
前景
长效及口服制剂是趋势
GLP-1受体激动剂除了具有促进胰岛素分泌作用,亦可抑制餐后胰高血糖素的分泌,延缓肠排空和抑制食欲。而第一代GLP-1受体激动剂半衰期短,在血液中迅速降解,因此研发长效制剂及口服用药是今后的主攻方向。
2014年4月15日,FDA批准了葛兰素史克研发的每周一次皮下注射的长效GLP-1类似物阿必鲁肽(Tanzeum);2014年9月18日,FDA批准了礼来研发的每周一次的长效GLP-1类似物度拉糖肽(Trulicity)上市;2017年12月5日,FDA批准了诺和诺德研发的每周一次皮下注射的长效GLP-1类似物索马鲁肽(Ozempic)。
GLP-1受体激动剂及类似物优点是有良好心血管收益及体重控制效果,不产生低血糖危象,但是针对利拉鲁肽、艾塞那肽患者使用跟踪研究表明,经过半年治疗后,两种药物坚持治疗率仅为60%,到12个月下降到30%,从而导致市场效益下滑。注射剂具有治疗成本高、操作不方便、风险高于口服剂的特征,导致了患者依从性差的后果。因此,开发非注射用药治疗快速增长的糖尿病,仍是迫在眉睫。
国内首个申请上市的长效GLP-1受体激动剂是豪森药业的洛塞那肽。目前,礼来的度拉糖肽的临床申请处于审评阶段,诺和诺德的索马鲁肽注射液已于2016年9月获批临床。此外,诺和诺德在国内提交的口服索马鲁肽片临床申请已经在审批中。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030