https://www.cphi.cn 2024-04-19 16:56 来源:药智网 作者:渡
干涸的沙漠中,无数创新药企前赴后继,争当苦行僧,艰难寻找下一片绿洲。
这其中,有的早已经失去方向、倒在茫茫戈壁滩上;有的却能镇定自若、处之泰然,依旧往着创新的方向坚定前行,恒瑞就是其中一员。
4月17日晚,恒瑞医药发布2023年财报,营业收入228.2亿元,同比增7.26%,扣非净利润41.41亿元,同比增长21.46%。
值得注意的是,其创新药收入106.37亿元,占总营收47%。可见创新转型初见成效,恒瑞已渐渐走出转型阵痛期。
无独有偶,不仅在年报中呈现创新成果,恒瑞近期在创新药方面的动作可谓左右开弓、上下齐动。
近期,恒瑞医药已有3款产品获得美国FDA快速通道资格认定,2024年仅过去了3个多月,恒瑞便以以迅雷不及掩耳之势占领创新高地,成为探险路上最亮眼的星。
一段关于恒瑞更有魅力的故事。恒瑞医药正以新的姿态,大步迈入全面突破的创新出海新阶段。
01
16款创新药上市
做时间积累的事。一直以来,恒瑞医药专注于抗肿瘤、代谢性疾病、自身免疫疾病、呼吸系统疾病、神经系统疾病等领域进行新药研发,据恒瑞医药2023年财报披露,公司已在中国上市自研创新药16款1类创新药、4款自研2类新药。
其中,3款1类创新药(阿得贝利单抗、磷酸瑞格列汀、奥特康唑)、4款2类新药(盐酸右美托咪定鼻喷雾剂、醋酸阿比特龙纳米晶、盐酸伊立替康脂质体、恒格列净二甲双胍缓释片)于2023年获批上市。
技术平台方面,恒瑞在美国、欧洲、澳大利亚、日本和中国多地设立了14个研发中心,建立了一批具有自主知识产权、国际领先的新技术平台,覆盖蛋白水解靶向嵌合物(PROTAC)、分子胶、抗体偶联药物(ADC)等多种药物形式。
不仅如此,恒瑞以近十年累计研发投入超300亿元,位居国内同行业前列。据2023年财报显示,2023年研发投入高达61.5亿元,占营收收入比重27%。
从研发管线来看,恒瑞正临床开发的自主创新产品90+,近300项临床试验在国内外开展,12项临床推进至三期。
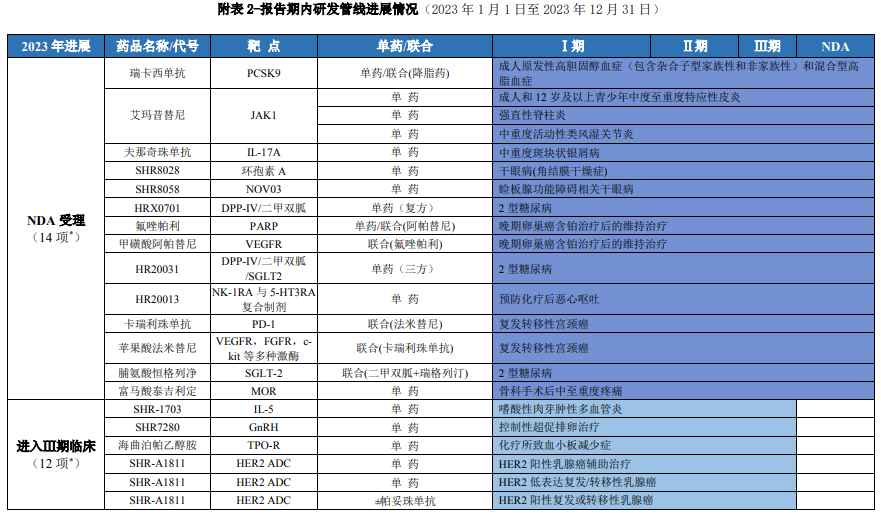
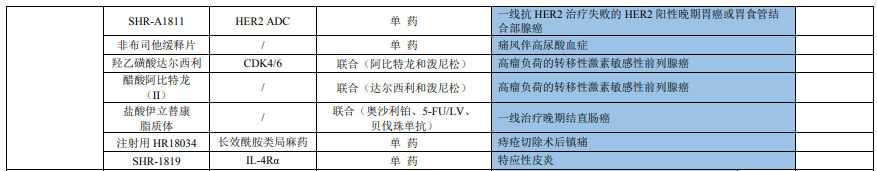
图1截至2023年12月31日,恒瑞医药部分管线进展
图片来源:恒瑞医药2023年财报
卡瑞利珠单抗
人源化PD-1单克隆抗体,能够与PD-1特异性结合,阻断PD-1与其配体的相互作用,使得T细胞恢复针对肿瘤免疫应答,达到治疗肿瘤的效果。
卡瑞利珠单抗已有9项适应症获批上市,2023年12月,卡瑞利珠单抗联合法米替尼治疗既往经含铂化疗失败的复发或转移性宫颈癌适应症上市申请获CDE受理。
氟唑帕利
作为国内第一个获批上市的自主研发PARP抑制剂,氟唑帕利具有独特的三氟甲基结构,该结构可使药物分子在体内不容易被代谢,2023年年度报告25/246从而保持药效的长期稳定性,组织滞留性更好。
2024年3月,氟唑帕利单药或联合阿帕替尼治疗gBRCA突变的HER2阴性乳腺癌被CDE纳入突破性治疗品种名单。
02
闯关FDA,屡创佳绩
作为国内医药一哥,恒瑞医药的一举一动备受市场关注,而恒瑞也用超强的创新力量,回复市场的热切期待,这其中包含2024年开年以来,恒瑞频频获得美国FDA认可:3款ADC创新药获得快速通道资格认定。
今年1月,恒瑞医药发布公告称,自主研发的HER3抗体偶联药物(ADC)创新药注射用SHR-A2009获得美国FDA授予快速通道资格(FTD),用于治疗经第三代EGFR酪氨酸激酶抑制剂和含铂化疗后疾病进展的EGFR突变的转移性非小细胞肺癌。
这不仅是恒瑞历史上第一款获得美国FDA快速通道资格认定的创新药,也是其自主研发的一款以HER3为靶点的抗体药物偶联物。值得注意的是,全球尚未有同类药物获批上市,快速通道资格认定无疑为该款药物插上加快推进临床试验及上市的翅膀。
此后,恒瑞火速开启FDA快速通道资格的大门,其自主研发的CD79bADC创新药注射用SHR-A1912、TROP-2ADC创新药注射用SHR-A1921先后获得快速通道资格认定,分别治疗既往接受过至少2线治疗的复发/难治性弥漫大B细胞淋巴瘤、铂耐药复发上皮性卵巢癌,欲拿下多样癌种。
每月1款创新药拿下快速通道资格认定的背后,是恒瑞模块化ADC创新平台HRMAP十年的厚积薄发:该平台能够快速合成各类ADC分子进行筛选,包含多种靶向抗体、多种机制的毒素、多种连接子和定点连接技术。

图2恒瑞ADC技术平台——HRMAPO
图片来源:太平洋证券
目前,恒瑞已有包括SHR-A1912在内的9个新型、具有差异化的ADC分子成功获批临床,5款产品实现国际同步开发。
为何恒瑞对ADC创新药情有独钟?这与ADC药物独特的治疗效果有关。
作为继化疗、靶向和免疫时代后又一类新型抗肿瘤药物,ADC药物既有抗体的高靶向性又有化疗药物的强杀伤力,成为新型抗癌药物明星。
不仅如此,近年来ADC药物屡屡显示其市场威力。据太平洋证券研报数据统计,全球已上市ADC药物销售总额呈快速增长趋势,从2017年的16亿到2022年的79亿美元,预测2023-2030年全球市场将以29.8%的复合增长率高速发展。
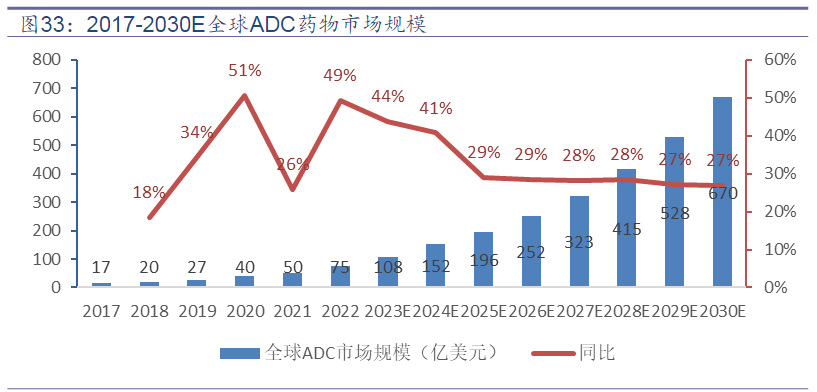
图32017-2030E全球ADC药物市场规模
图片来源:太平洋证券
03
国际化:自主研发与开放合作并重
国际战略方面,恒瑞医药坚持自主研发与开放合作并重,在内生发展的基础上加强国际合作,包括以现有产品为主的制剂出口、产品引进和对外许可授权及积极开展海外临床。
制剂出口
已在欧美日获得包括注射剂、口服制剂和吸入性麻 醉剂在内的20多个注册批件,据恒瑞官网披露,公司产品已进入包括欧美日规范市场在内的40余个国家。
钆特酸葡胺注射液、钆布醇注射液、碘克沙醇注射液获准在美国销售,后二者为美国FDA批准上市的首仿产品,其中碘克沙醇为2022年美国市场短缺产品。
产品引进和对外许可
通过与美国、韩国、德国、印度公司合作,公司将卡瑞利珠单抗、吡咯替尼、HRS-1167等多个具有自主知识产权的创新药对海外授权,交易总金额超40亿美元。
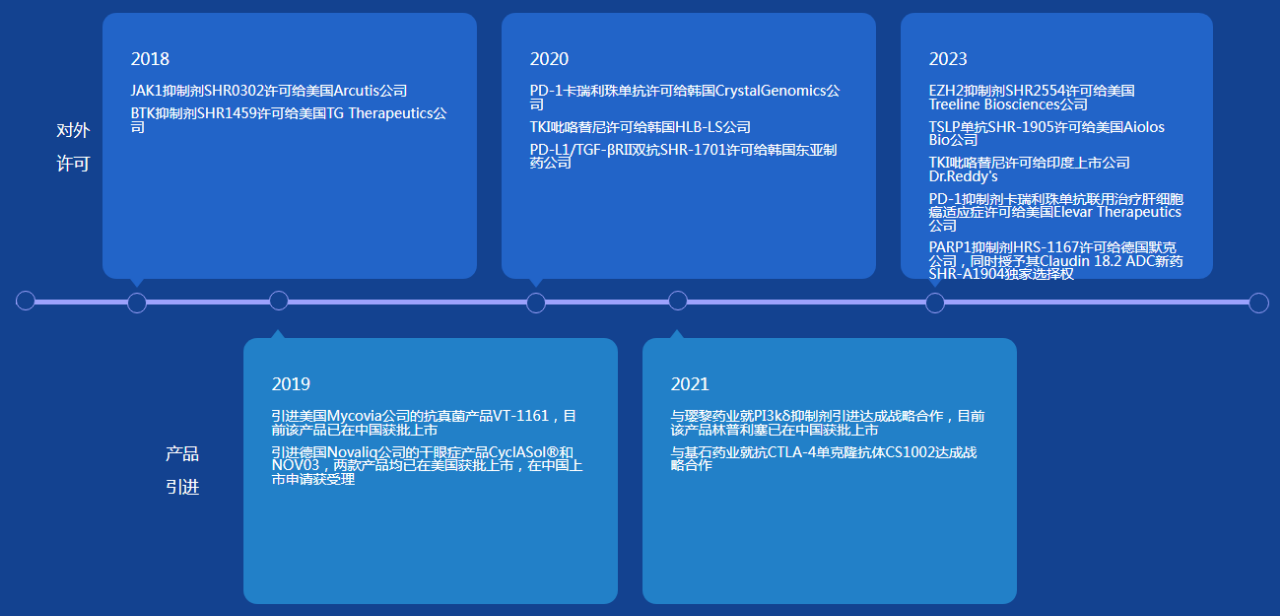
图42018年-2023年,恒瑞医药产品引进与对外许可项目
图片来源:恒瑞医药官网
海外临床
氟唑帕利、海曲泊帕、SHR0302等近20项国际临床试验在海外开展。卡瑞利珠单抗、海曲泊帕乙醇胺片、Edralbrutinib片3款创新药获美国FDA孤儿药认定,3款ADC创新药获得快速通道资格认定,将加速在美临床试验及上市注册。
04
结语
危机时刻,恒瑞始终保持清醒头脑与正确方向,是医药寒冬中最难能可贵的能力。
不惧风雨、砥砺前行,相信以恒瑞为首的中国药企,必将用实力和担当挺起中国医药脊梁,锚定目标向着深海更加坚定地出发。
参考来源:
1、恒瑞医药官微、官网、2023年年报
2、《ADC鏖战引领精准化疗新时代》,太平洋证券
3、《恒瑞医药(600276.SH)公司深度报告:创新药持续兑现,经营步入新周期》,国海证券
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030